
華中科技大學(xué)同濟(jì)醫(yī)學(xué)院基礎(chǔ)醫(yī)學(xué)院生物化學(xué)與分子生物學(xué)系、華中科技大學(xué)細(xì)胞架構(gòu)研究中心丁彬彬教授課題組于2023年3月10號(hào)在Cell Reports在線發(fā)表了題為“Coronavirus Subverts ER-phagy by Hijacking FAM134B and ATL3 into p62 Condensates to Facilitate Viral Replication”的研究論文,,揭示冠狀病毒輔助蛋白ORF8通過相分離抑制內(nèi)質(zhì)網(wǎng)自噬,,促進(jìn)病毒復(fù)制的新機(jī)制。
內(nèi)質(zhì)網(wǎng)是細(xì)胞中分布最廣的動(dòng)態(tài)多形性細(xì)胞器,,橫跨整個(gè)細(xì)胞質(zhì),,其功能是幫助蛋白折疊、合成分泌蛋白,、脂質(zhì),,促進(jìn)藥物代謝、鈣信號(hào)傳導(dǎo)和細(xì)胞器互作,。內(nèi)質(zhì)網(wǎng)自噬(ER-phagy)是自噬體選擇性的將內(nèi)質(zhì)網(wǎng)包裹,,利用溶酶體將其降解的一種細(xì)胞應(yīng)激反應(yīng)。已有的研究發(fā)現(xiàn)內(nèi)質(zhì)網(wǎng)自噬可通過內(nèi)質(zhì)網(wǎng)定位的受體FAM134B,,RTN3L,,CCPG1,SEC62,,TEX264和ATL3與自噬標(biāo)記蛋白LC3結(jié)合,,介導(dǎo)自噬體對片狀或管狀內(nèi)質(zhì)網(wǎng)的識(shí)別和包裹。黃病毒(登革病毒,、寨卡病毒等)利用其編碼的蛋白酶降解受體FAM134B從而抑制內(nèi)質(zhì)網(wǎng)自噬,。冠狀病毒可重塑內(nèi)質(zhì)網(wǎng)膜系統(tǒng)形成病毒雙層膜復(fù)制細(xì)胞器(DMVs,double membrane vesicles),。但是關(guān)于內(nèi)質(zhì)網(wǎng)自噬在冠狀病毒DMVs形成中是否發(fā)揮作用尚不清楚,。
自噬蛋白p62在細(xì)胞中存在兩種狀態(tài):一種是作為自噬配體介導(dǎo)選擇性自噬,,另一種是與泛素結(jié)合形成相分離。然而目前對于p62相分離的功能研究不是很多,,p62相分離與內(nèi)質(zhì)網(wǎng)自噬是否有關(guān)還不清楚,。
在本研究中,丁彬彬教授團(tuán)隊(duì)發(fā)現(xiàn)冠狀病毒輔助蛋白ORF8具有相分離特性,,通過分析ORF8免疫共沉淀/蛋白質(zhì)譜結(jié)果,,發(fā)現(xiàn)ORF8與自噬蛋白p62相互作用并形成相分離;ORF8與內(nèi)質(zhì)網(wǎng)自噬受體FAM134和ATL3相互作用,,將受體劫持進(jìn)ORF8/p62相分離中,,從而阻止內(nèi)質(zhì)網(wǎng)自噬的發(fā)生,確保病毒可以重塑內(nèi)質(zhì)網(wǎng)形成DMVs,,利于病毒復(fù)制,;進(jìn)一步的研究發(fā)現(xiàn)ORF8通過二聚體的形式與FAM134B和ATL3相互作用,但是其二聚對于與p62形成相分離是非必須,。
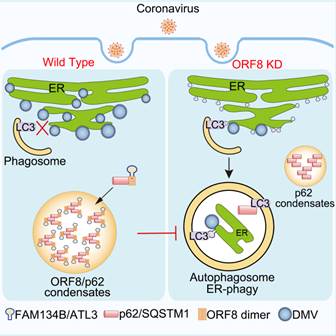
模式圖:ORF8與p62形成相分離,,劫持FAM134B和ATL3,抑制內(nèi)質(zhì)網(wǎng)自噬,。
本研究將p62相分離與內(nèi)質(zhì)網(wǎng)自噬首次聯(lián)系起來,,揭示了病毒如何利用相分離劫持內(nèi)質(zhì)網(wǎng)自噬受體,從而驅(qū)動(dòng)病毒復(fù)制的全新機(jī)制,,為后續(xù)更深入的探索p62相分離和內(nèi)質(zhì)網(wǎng)自噬在病毒感染中的作用及研究開發(fā)抗病毒藥物提供理論基礎(chǔ)和潛在靶點(diǎn),。
基礎(chǔ)醫(yī)學(xué)院博士研究生譚萱、湖北疾病預(yù)防控制中心蔡昆和藥學(xué)院李佳佳為本文共同第一作者,,丁彬彬教授和武漢大學(xué)生命科學(xué)院覃雅麗教授為論文共同通訊作者,。該研究得到國家自然科學(xué)基金重大研究計(jì)劃“細(xì)胞器互作網(wǎng)絡(luò)及其功能研究”培育項(xiàng)目和國家自然科學(xué)基金聯(lián)合基金重點(diǎn)支持項(xiàng)目的資助。










 English
English


